Modelo atómico de Bohr.
Bohr describió el átomo de hidrógeno con un protón en el núcleo, y girando a su alrededor un electrón. En éste modelo los electrones giran en órbitas circulares alrededor del núcleo; ocupando la órbita de menor energía posible, o sea la órbita más cercana posible al núcleo.
Enlace iónico.
En química y en física, un enlace iónico o electrovalente es el resultado de la presencia de atracción electrostática entre los iones de distinto signo.
Concepto:
Ácido.
Un ácido es considerado tradicionalmente como cualquier compuesto químico que, cuando se disuelve en agua, produce una solución con una actividad de catión hidronio mayor que el agua pura, esto es, un pH menor que 7.
Base.
Una base o álcali es cualquier sustancia que presente propiedades alcalinas. En primera aproximación es cualquier sustancia que en disolución acuosa aporta iones OH− al medio. Un ejemplo claro es el hidróxido de potasio, de fórmula KOH.
domingo, 28 de enero de 2018
sábado, 27 de enero de 2018
lunes, 22 de enero de 2018
domingo, 21 de enero de 2018
SEMANA 2 INVESTIGACIÓN SEMANAL.
COMPUESTOS INORGÁNICOS ÓXIDOS, ÁCIDOS, HIDRÓXIDOS Y SALES.
¿Qué es un compuesto inorgánico?
Son sustancias inertes o muertas, y se caracterizan por no contener carbono, como por ejemplo la cal, la sal de cocina, acido de batería y otras, que son estudiadas por la Química inorgánica. Hay ciertos compuestos que contienen carbono y se consideran como inorgánicos, dado que no contienen enlaces carbono-carbono y que sus propiedades son semejantes a este tipo de compuestos, entre los cuales está el monóxido de carbono (CO) y el dióxido de carbono (CO2).
Otros ejemplos de estos compuestos son: agua (H2O), cloruro de sodio (NaCl), monóxido de Nitrógeno (NO), ácido clorhídrico (HCl), hidróxido de sodio (NaOH), etc.
Los óxidos
Son compuestos inorgánicos binarios (que tienen dos elementos), que se obtienen a partir de la combinación de un Metal y el Oxígeno molecular gaseoso. En forma simbólica dicho enunciado:

Son compuestos inorgánicos binarios (que tienen dos elementos), que se obtienen a partir de la combinación de un Metal y el Oxígeno molecular gaseoso. En forma simbólica dicho enunciado:

ácidos

El hidrogeno es el elemento químico fundamental de los ácidos inorgánicos o ácidos minerales y existen dos grupos: oxácidos e hidrácidos.
Se les conoce también como anhídridos y óxidos no-metálicos, y resultan de la combinación del oxígeno (O) con un no-metal (NM), mediante enlace covalente. Para nombrarlos se aplica la nomenclatura de proporciones (mono, di, tri...).
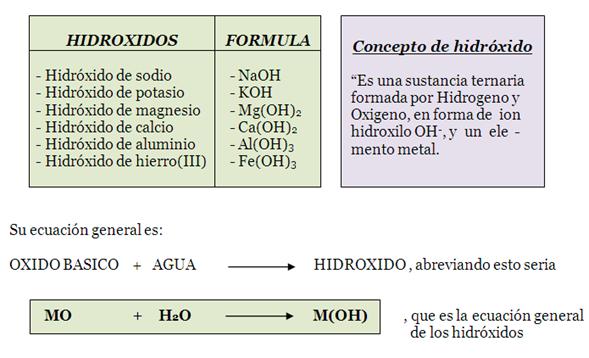
hidróxidos.
Conocidos también como bases. Estas sustancias son ternarias y resultan de combinar un oxido básico con agua; se caracterizan por llevar siempre, además del elemento metal, una molécula llamada ion hidroxilo u oxidrilo, formada por el oxígeno e hidrogeno (OH)-; se nombran usando la nomenclatura de Stock. A continuación algunos ejemplos de estos compuestos.
Sales.
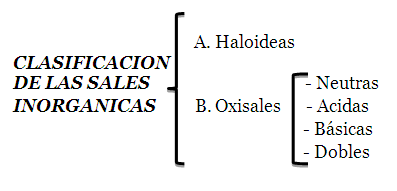
Las sales son cristales y solubles en agua, por lo general. Son sustancias binarias, ternarias y cuaternarias. Existen 2 tipos principales de ellas:
- a. Sales haloideas.
- b. Sales oxisales. Estas se clasifican en 4 tipos: sales neutras, ácidas, básicas y sales dobles.
Las diferentes sales resultan de la reacción entre un ácido y una base, siendo esta reacción de neutralización completa o bien parcial, y en todos los casos se produce también agua (4).
PROPIEDADES DE LAS SALES
Propiedades de las sales.
|
SEMANA 2 SESIÓN 4
Semana2
SESIÓN
4
|
PRIMERA
UNIDAD. Suelo, fuente de nutrientes para las plantas
|
contenido temático
|
Propiedades generales de las sales
Macro y micronutrientes.
|
Aprendizajes esperados
del grupo
|
Conceptuales:
4. Clasifica los tipos de
compuestos inorgánicos presentes en el suelo e identifica cuales proveen de
nutrientes a las plantas. (N3)
Procedimentales
·
Desarrolle su habilidad en la búsqueda de información
·
Desarrolle su capacidad
de observación al experimentar
·
Reconozca que los
experimentos son una forma de obtener información y de acercarse al
conocimiento de la realidad.
·
Identifique las
variables por observar en un experimento.
Actitudinales
·
Respeto en el manejo responsable del suelo.
·
Cooperación y solidaridad con los integrantes de su equipo
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Materiales generales
|
De Laboratorio:
Material: Vaso de precipitados 250 ml, probeta graduada, capsula de porcelana,
probador de conductividad, balanza.
Sustancias: Ácido clorhídrico, nitrato de plata, agua destilada. Suelo del cerro de
Zacaltepetl. Abajo,(A)En medio(E),Arriba(A).
Didáctico:
-
Presentación, escrita electrónicamente.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Desarrollo del
Proceso
|
FASE DE
APERTURA
El Profesor de acuerdo a su Planeación de clase
presenta las preguntas siguientes:
El Profesor de acuerdo a su Planeación de clase presenta
las preguntas siguientes:
Macronutrientes N.P,K,Ca,Mg.S micronutrientes Fe,Mn,,Zn,Cu, B,Mo
Se
emplea la técnica Discusión en equipo, para procesar su información,
sintetizar y aprender del texto.
Cada
equipo lee diferente contenido sobre las preguntas.
FASE DE DESARROLLO
FASE
DE DESARROLLO
Propiedades
organolépticas del suelo:
-
Colocar una muestra del suelo de abajo en la
capsula de porcelana, observar su
color, forma, y textura (con
dos dedos humedecidos en agua detectar en la muestra de cada suelo si es
arenoso, arcillo o limoso
Observaciones:
Propiedades
Físicas del Suelo:
Densidad
-
En la probeta graduada Pesar 10 mililitros de
cada suelo, calcular su densidad (masa
g / volumen ml)
-
En la
probeta graduada Medir la porosidad de cada suelo adicionando agua hasta que
se forme un espejo en la parte superior del suelo Porosidad ml de agua
-
Colocar una muestra da cada suelo (una por
una) y determinar su conductividad eléctrica en seco y en húmedo.
Observaciones:
Características
Químicas del suelo
Determinación de cloruros y carbonatos en el suelo.
Los alumnos desarrollan las
actividades de acuerdo a las indicaciones del Profesor
Identificación
de carbonatos:
-Colocar
una muestra del suelo de abajo en la capsula de porcelana y agregar con la
pipeta una gota del ácido clorhídrico. Anotar las observaciones. Repetir lo
anterior con el suelo de en medio y arriba.
Identificación
de Cloruros.
Colocar
una muestra del suelo en el vaso de precipitados y agregar 20 ml de agua
destilada, agitar y filtrar la muestra en el tubo de ensaye agregar unas
gotas del nitrato de plata y observar los cambios.
Observaciones:
Conclusiones:
¿Cuál
sustancia mostró mayor conductividad
eléctrica? El de abajo
¿Por
qué? Por las sales.
¿Cuál
sustancia mostró menor conductividad eléctrica? El de arriba
FASE DE CIERRE
Los equipos
presentan su información a los demás.
Al final de las presentaciones se lleva a cabo una
discusión extensa, en la clase con el profesor, de lo que se aprendió.
Actividad
Extra clase:
Cada equipo seleccionará un tipo de frijol para llevar
a cabo la Germinación del mismo en cada tipo del suelo del Cerro de
Zacaltepetl, A,E y A.
Los alumnos llevaran la información a su casa
e indagaran los temas siguientes de acuerdo al cronograma macro y
micronutrientes.
http://tablaperiodica.in/tabla-periodica-interactiva-2012/
Elaboraran su informe, en un documento electrónico,
para publicar los resultados en su Blog.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Evaluación
|
Informe de la actividad
publicada en el Blog
Resumen de la indagación
bibliográfica.
Actividad de Laboratorio. Tabulación y graficas de
Germinación del frijol.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Suscribirse a:
Comentarios (Atom)




































